Detection and Field Monitoring of Water Spinach Canker
-
摘要:
目的 蕹菜是我国南方重要的经济作物,近年来随着蕹菜种植面积不断扩大,由穿孔黄单胞菌(Xanthomonas perforans)引起的蕹菜溃疡病日趋严重,对生产造成了巨大损失。建立高效快捷的蕹菜溃疡病菌检测技术,可为有效防控病害奠定基础。 方法 采用普通PCR检测技术,针对蕹菜溃疡病菌X. perforans基因组中特有序列TC2-1_002562(编码噬菌体终止酶大亚基家族蛋白)和TC2-1_002580(编码噬菌体家族蛋白)设计两对特异性检测引物,在同一个PCR体系中达到了快速检测蕹菜溃疡病菌的目的。 结果 建立的PCR检测方法可操作性强,对蕹菜溃疡病菌具有良好的特异性。利用特异性引物对来自广东多个地区的蕹菜植株、土壤和水体进行病原菌分子检测,发现第一批样本仅在5份来自东莞的蕹菜叶片上检测到病原菌,第二批样本分别在土壤、水体和植株上检测到病原菌。 结论 所建立的PCR检测方法能快速检测穿孔黄单胞菌,可用于对蕹菜溃疡病的早期诊断。该病在东莞、深圳等地呈普遍发生态势,田间检测结果表明,病害发展迅速,留种蕹菜种苗或种子很可能是该病的初侵染源,种植环境的水、土壤也是病害循环的重要环节,这对于今后进一步研究病害循环规律、制定针对性防控策略具有重要意义。 Abstract:Objective An efficient and rapid detection method was developed to monitor the spread of a newly discovered bacterial canker disease infected by Xanthomonas perforans that seriously impacted the production of water spinach (Ipomoea aquatica), a recently introduced and increasingly important cash crop in southern China. Method Two pairs of primers were designed to detect X. perforans based on the specific sequences in the genomes including TC2-1_002562 and TC2-1_002580, which encode a phage terminator large subunit family protein and a phage family protein, respectively. The applicability of the proposed methodology with a single PCR reaction was verified. Result The newly developed PCR method exhibited a high specificity for detecting X. perforans. In the first sampling batch of water spinach plants, planting soils, and water collected from regions in Guangdong Province, the pathogen was only detected in 5 specimens of water spinach leaves from Dongguan. However, during the subsequent second sampling 10 days later, the pathogen was found in numerous specimens from all sources. Conclusion The established PCR method could rapidly detect X. perforans for early disease diagnosis on water spinach. As the field monitoring indicated, the endemic was prevalent in Dongguan and Shenzhen, possibly some other localities, but spreading fast. The origin of the infection might come from the stored water spinach seedlings and/or seeds. The area water and soil could also link to the spread of the disease. Urgent study to timely develop effective prevention and control measures is in order. -
Key words:
- Water spinach /
- canker /
- Xanthomonas perforans /
- PCR detection
-
图 1 XP-F1/R1和XP-F2/R2的特异性检验结果
M:DL2000 DNA marker;TC2-1、829-1代表来源于广东和福建的蕹菜溃疡病病原菌,Xad代表红掌细菌性疫病病原菌,Xcc代表野油菜黄单胞杆菌,Xcm代表芒果露水斑病菌,Xac代表柑橘溃疡病菌,Xoo代表水稻白叶枯病菌,Psa代表豌豆细菌性疫病菌,Pst代表丁香假单胞菌。
Figure 1. Specificity of detection on X. perforans using XP-F1/R1 and XP-F2/R2 primers
M: DL2000 DNA marker; TC2-1 and 829-1: X. perforans strains isolated from diseased water spinach leaves in Guangdong and Fujian, respectively; Xad: X. axonopodis pv. dieffenbachiae ; Xcc: X. campetris pv. campetris; Xcm: X. citri pv. mangiferaeindicae; Xac: X. citri subsp. citri; Xoo: X. oryzae pv. oryzae; Psa: P. syringae pv. pisi; Pst: P. syringae pv. tomato.
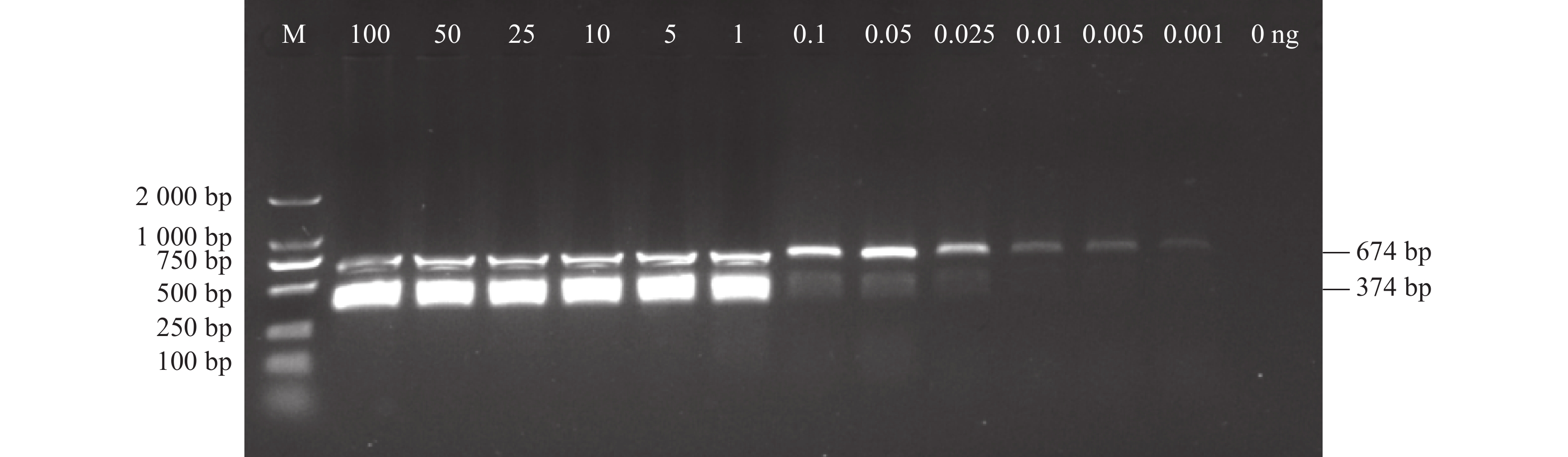
图 2 XP-F1/R1和XP-F2/R2的灵敏性检验结果
M:DL2000 DNA marker;不同孔代表模板为不同浓度的蕹菜溃疡病病原菌X. perforans TC2-1基因组DNA。
Figure 2. Sensitivity of detection on X. perforans using XP-F1/R1 and XP-F2/R2 primers
M: DL2000 DNA marker; different concentrations of X. perforans TC2-1 gDNA were used as templates for PCR amplification.
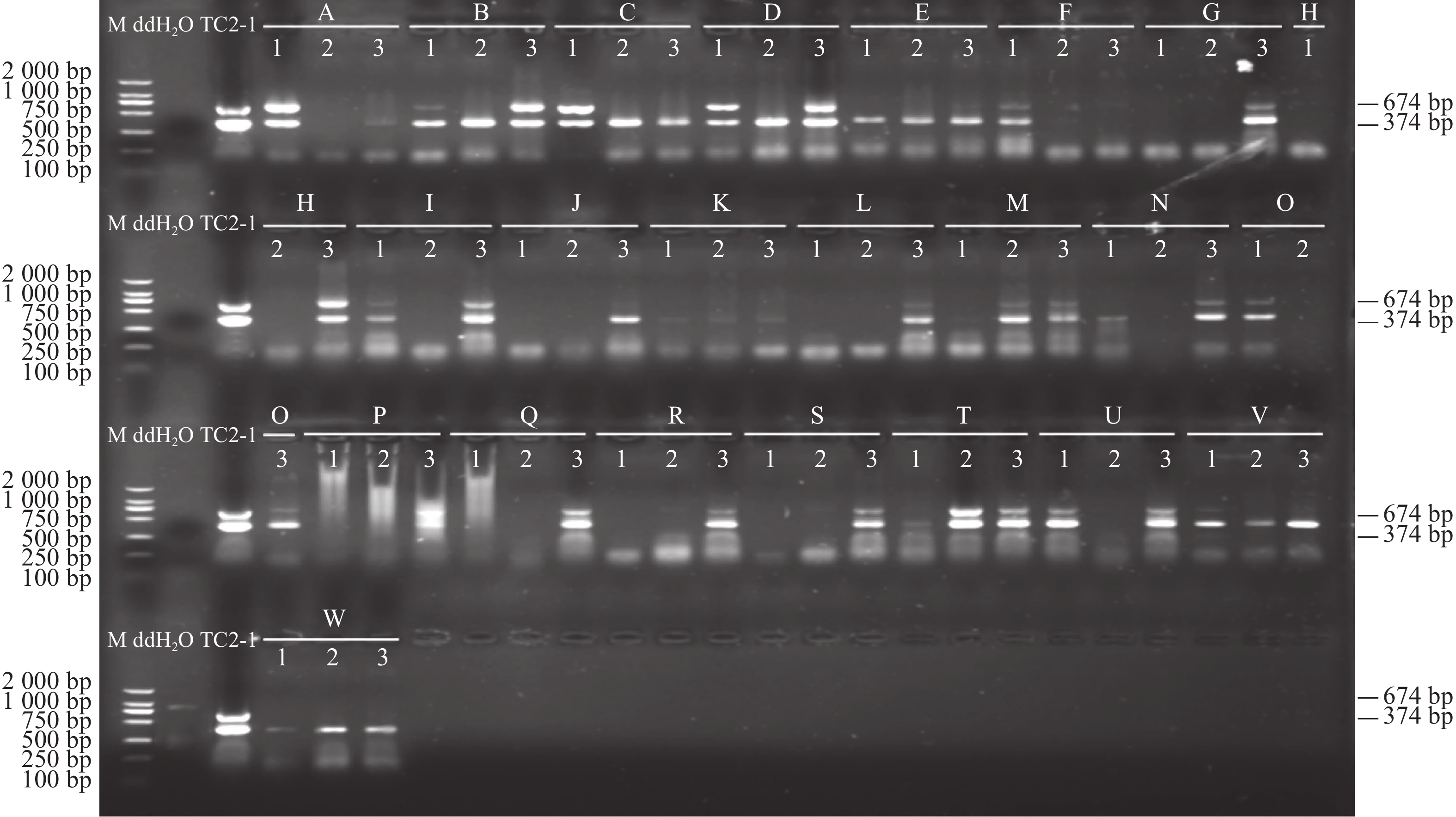
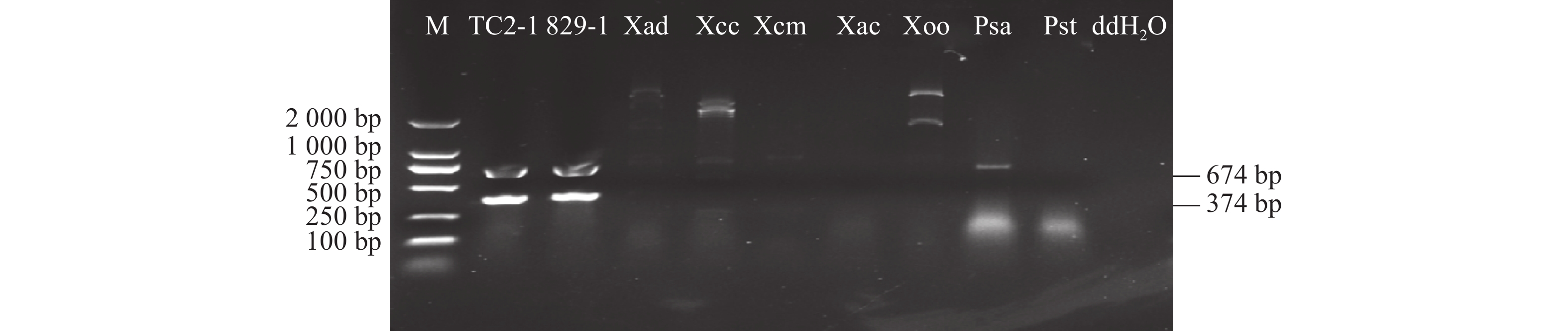
图 3 利用XP-F1/R1和XP-F2/R2特异性引物对第一批田间样本的PCR检测结果
M:DL2000 DNA marker;ddH2O:空白对照;TC2-1:以X. perforans TC2-1基因组DNA为模板进行PCR作为阳性对照;A—V:对应表1中不同采样地点的田间样本;1、2、3分别代表土样、水样和蕹菜叶片。
Figure 3. Detection on 1st batch field samples using XP-F1/R1 and XP-F2/R2 primers
M: DL2000 DNA marker; ddH2O: blank control; TC2-1: X. perforans TC2-1 gDNA used for PCR template to serve as positive control; A to V: PCR amplicons with different templates corresponding to sampling locations shown in Table 1; 1, 2, and 3: soil, water, and water spinach leaf samples, respectively.
图 4 利用XP-F1/R1和XP-F2/R2特异性引物对第二批田间样本的PCR检测结果
M:DL2000 DNA marker;ddH2O:空白对照;TC2-1:以X. perforans TC2-1的基因组DNA作为模板进行PCR作为阳性对照;A—W:对应表2中不同采样地点的田间样本;1、2、3分别代表土样、水样和蕹菜叶片。
Figure 4. Detection on 2nd batch field samples using XP-F1/R1 and XP-F2/R2 primers
M: DL2000 DNA marker; ddH2O: blank control; TC2-1:X. perforans TC2-1 gDNA used for PCR template to serve as positive control; A to W: PCR amplicons with different templates corresponding to sampling locations shown in Table 2; 1, 2, and 3: soil, water, and water spinach leaf samples, respectively.
表 1 第一批样本采样信息及检测结果(2022年7月5日)
Table 1. Information and detection of canker disease in 1st sampling on July 5, 2022
序号
No.采样时期
Plant stage采样地点
Sampling location土样
Soil sample水样
Water sample叶样
Leaf sampleA 苗期 深圳市光明区玉塘街道玉律社区望家欢菜场 1(−) 1(−) 1(−) B 苗期 深圳市宝安区航城街道黄麻布社区湖尔美菜场 1(−) 1(−) 1(−) C 临近采收期 深圳市光明区玉塘街道玉律社区望家欢菜场 1(−) 1(−) 1(−) D 临近采收期 深圳市宝安区航城街道黄麻布社区湖尔美菜场 1(−) 1(−) 1(−) E 苗期 东莞市高埗镇三联村三队对面海 0 0 1(−) F 苗期 东莞市高埗镇保安围村三队高低卅贝 0 0 1(−) G 苗期 东莞市万江区大汾社区万江家兴蔬菜种植专业合作社 1(−) 1(−) 1(−) H 苗期 东莞市万江区大汾社区万江家兴蔬菜种植专业合作社 1(−) 1(−) 1(−) I 苗期 东莞市谢岗镇黎村担水沥 1(−) 1(−) 1(+) J 苗期 东莞市谢岗镇黎村担水沥 1(−) 1(−) 1(+) K 苗期 东莞市大岭山镇大沙村浪尾浦蔬菜生产基地 1(−) 1(−) 1(−) L 苗期 东莞市大岭山镇大沙村浪尾浦蔬菜生产基地 1(−) 1(−) 1(−) M 临近采收期 东莞市东坑镇初坑村一队 1(−) 1(−) 1(−) N 临近采收期 东莞市东坑镇农业园正门益品原农场 1(−) 1(−) 1(−) O 苗期 东莞市桥头镇石水口村牛埔 1(−) 1(−) 1(−) P 苗期 东莞市桥头镇迳联社区草埔 1(−) 1(−) 1(−) Q 苗期 东莞市麻涌镇沥黎滘村菜地 1(−) 1(−) 1(+) R 苗期 东莞市麻涌镇蒲基村菜地 1(−) 1(−) 1(+) S 苗期 东莞市石碣镇四甲村叶屋基生产基地 1(−) 1(−) 1(−) T 苗期 东莞市石碣镇四甲村叶屋基生产基地 1(−) 1(−) 1(−) U 苗期 东莞市道滘镇蔡白村菜地 1(−) 1(−) 1(−) V 苗期 东莞市道滘镇大鱼沙村菜地 1(−) 1(−) 1(+) 表中数字代表样本数,+代表检测结果为阳性,−代表检测结果为阴性。表2同。
The numbers in the table represent the number of samples, + represents a positive test result, and −represents a negative test result. Same for table 2.表 2 第二批样本采样信息及检测结果(2022年7月15日)
Table 2. Information and detection on canker disease in 2nd sampling on July 15, 2022
序号
No.采样时期
Plant stage采样地点
Sampling location土样
Soil sample水样
Water sample叶片
Leaf sampleA 苗期 深圳市光明区新湖街道新羌社区绿田菜场 1(+) 1(−) 1(+) B 临近采收期 深圳市光明区新湖街道新羌社区绿田菜场 1(+) 1(+) 1(+) C 临近采收期 深圳市宝安区燕罗街道燕川菜场 1(+) 1(+) 1(+) D 收获期 东莞市高埗镇三联村三队对面海 1(+) 1(+) 1(+) E 收获期 东莞市高埗镇保安围村三队高低卅贝 1(+) 1(+) 1(+) F 临近采收期 东莞市万江区大汾社区万江家兴蔬菜种植专业合作社 1(+) 1(−) 1(−) G 临近采收期 东莞市万江区大汾社区万江家兴蔬菜种植专业合作社 1(−) 1(−) 1(+) H 临近采收期 东莞市谢岗镇黎村担水沥 1(−) 1(−) 1(+) I 临近采收期 东莞市谢岗镇黎村担水沥 1(+) 1(−) 1(+) J 临近采收期 东莞市大岭山镇大沙村浪尾浦蔬菜生产基地 1(−) 1(−) 1(+) K 临近采收期 东莞市大岭山镇大沙村浪尾浦蔬菜生产基地 1(+) 1(+) 1(+) L 苗期 东莞市东坑镇初坑村一队 1(−) 1(−) 1(+) M 苗期 东莞市东坑镇农业园正门益品原农场 1(−) 1(+) 1(+) N 临近采收期 东莞市桥头镇石水口村牛埔 1(+) 1(−) 1(+) O 临近采收期 东莞市桥头镇迳联社区草埔 1(+) 1(−) 1(+) P 临近采收期 东莞市麻涌镇沥黎滘村菜地 1(−) 1(−) 1(+) Q 临近采收期 东莞市麻涌镇蒲基村菜地 1(−) 1(−) 1(+) R 临近采收期 东莞市石碣镇四甲村叶屋基生产基地 1(−) 1(−) 1(+) S 临近采收期 东莞市石碣镇四甲村叶屋基生产基地 1(−) 1(−) 1(+) T 临近采收期 东莞市道滘镇蔡白村菜地 1(+) 1(+) 1(+) U 临近采收期 东莞市道滘镇大鱼沙村菜地 1(+) 1(−) 1(+) V 临近采收期 东莞市厚街镇厚街村厚街菜地 1(+) 1(+) 1(+) W 临近采收期 东莞市厚街镇涌口村涌口菜地 1(+) 1(+) 1(+) -
[1] AMIN I, FUN C S. Determination of vitamin C, b-carotene and riboflavin contents in five green vegetables organically and conventionally grown [J]. Malaysian Journal of Nutrition, 2003, 9(1): 31−39. [2] HU M H, YUAN J H, YANG X E, et al. Study on nutraceutical properties of different cultivars Ipomoea aquatica Forsskal (‘Chunbai’ and ‘Liulv’) in an eutrophic water body [J]. Scientia Horticulturae, 2010, 124(3): 419−422. doi: 10.1016/j.scienta.2010.01.011 [3] LAWAL U, MEDIANI A, Maulidiani H, et al. Metabolite profiling of Ipomoea aquatica at different growth stages in correlation to the antioxidant and α-glucosidase inhibitory activities elucidated by 1H NMR-based metabolomics [J]. Scientia Horticulturae, 2015, 192: 400−408. doi: 10.1016/j.scienta.2015.06.036 [4] LAWAL U, MAULIDIANI M, SHAARI K, et al. Discrimination of Ipomoea aquatica cultivars and bioactivity correlations using NMR-based metabolomics approach [J]. Plant Biosystems, 2017, 151(5): 833−843. doi: 10.1080/11263504.2016.1211198 [5] DUKE J A, AYENSU E S. Medicinal plants of China[M]. Algonac, Mich. : Reference Publications, 1985. [6] TSENG C F, IWAKAMI S, MIKAJIRI A, et al. Inhibition of in vitro prostaglandin and leukotriene biosyntheses by cinnamoyl-beta-phenethylamine and N-acyldopamine derivatives [J]. Chemical & Pharmaceutical Bulletin, 1992, 40(2): 396−400. [7] MALALAVIDHANE T S, WICKRAMASINGHE S M D N, JANSZ E R. Oral hypoglycaemic activity of Ipomoea aquatica [J]. Journal of Ethnopharmacology, 2000, 72(1/2): 293−298. [8] PRASAD K N, DIVAKAR S, SHIVAMURTHY G R, et al. Isolation of a free radical-scavenging antioxidant from water spinach (Ipomoea aquatica Forsk) [J]. Journal of the Science of Food and Agriculture, 2005, 85(9): 1461−1468. doi: 10.1002/jsfa.2125 [9] MOURA M L, JACQUES M A, BRITO L M, et al. Tomato pith necrosis TPN caused by P. corrugata and P. mediterranea: severity of damages and crop loss assessment [J]. Acta Horticulturae, 2005(695): 365−372. [10] HU M, LI C H, ZHOU X F, et al. Microbial diversity analysis and genome sequencing identify Xanthomonas perforans as the pathogen of bacterial leaf canker of water spinach (Ipomoea aquatic) [J]. Frontiers in Microbiology, 2021, 12: 752760. doi: 10.3389/fmicb.2021.752760 [11] 胡宇如, 杨丙烨, 胡方平, 等. 蕹菜细菌性叶斑病的病原菌鉴定 [C]//中国植物病理学会2018年学术年会论文集, 2018: 369. [12] 张玲玲, 周洁, 秦曼丽, 等. 生姜青枯病病原菌的鉴定与PCR检测方法的建立 [J]. 西南大学学报(自然科学版), 2021, 43(9):10−20.ZHANG L L, ZHOU J, QIN M L, et al. Isolation and identification of the pathogen of ginger bacterial wilt and establishment of a PCR detection system [J]. Journal of Southwest University (Natural Science Edition), 2021, 43(9): 10−20.(in Chinese) [13] AIELLO D, SCUDERI G, VITALE A, et al. A pith necrosis caused by Xanthomonas perforans on tomato plants [J]. European Journal of Plant Pathology, 2013, 137(1): 29−41. doi: 10.1007/s10658-013-0214-7 [14] SCHWARTZ A R, POTNIS N, TIMILSINA S, et al. Phylogenomics of Xanthomonas field strains infecting pepper and tomato reveals diversity in effector repertoires and identifies determinants of host specificity [J]. Frontiers in Microbiology, 2015(6): 535. -
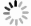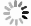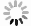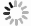






 下载:
下载: