Effects of Corn Meal and Flaxseed Oil Dietary Supplements on Fat Content in Milk and Rumen Microbial Flora of Dairy Cows
-
摘要:
目的 阐释日粮添加玉米粉与油脂诱导奶牛低乳脂情况下,奶牛瘤胃细菌菌群的变化情况。 方法 采用自身对照试验设计,选取4头体况相近、健康的泌乳期中国荷斯坦奶牛。试验开始前先以基础日粮预饲并以自身作对照。试验期奶牛日粮中添加玉米粉1.5 kg·头-1·d-1,添加胡麻油150 mL·头-1·d-1。预饲期为7 d,试验期为15 d,分析奶牛乳脂率及瘤胃细菌菌群变化情况。 结果 在饲料淀粉营养水平达到27%左右水平上额外添加胡麻油150 mL·头-1·d-1,连续添加15 d使奶牛的乳脂率极显著降低(P < 0.01),乳糖显著升高(P < 0.05),成功诱导奶牛乳脂降低。瘤胃细菌研究表明,在门水平上共检测到29个菌门,与对照组相比,玉米粉和油脂诱导乳脂降低后奶牛瘤胃导软壁菌门丰度显著降低(P < 0.05),放线菌门与浮霉菌门丰度极显著增加(P < 0.01);螺旋菌门丰度显著增加(P < 0.05)。在属水平上检测到389个菌属,其中110个菌属有显著差异(P < 0.05)。与对照组相比,试验组奶牛瘤胃乳酸菌杆菌属丰度极显著增加(P < 0.01),肠球菌属丰度极显著降低(P < 0.01),克里斯滕森菌属显著降低(P < 0.05),普雷沃菌属丰度显著增加(P < 0.05),毛螺旋菌极显著降低(P < 0.01),未注释毛螺旋菌属丰度显著增加,丁酸弧菌属-2(Butyrivibrio-2)丰度显著降低(P < 0.05),瘤胃球菌属-1丰度显著提高。 结论 日粮添加玉米粉与油脂诱导奶牛乳脂降低,瘤胃细菌菌群多样性未产生显著影响,但菌群结构及丰度发生了较大改变,产酸菌属与淀粉利用菌属增加显著。 Abstract:Objective Changes on the fat content of milk from and rumen microbial flora in dairy cows fed with corn meal and flaxseed oil supplemented forage were studied. Method In a self-control experimentation, 4 Chinese Holstein cows of similar physical conditions and normal lactation were fed on a daily diet added with 1.5 kg of corn meal and 150 mL per animal of flaxseed oil for 7 pre-trial days followed by 15 days for the test. Result In the feed containing approximately 27% starch, the dietary supplements significantly lowered the fat content (P < 0.01) with a significantly higher lactose content (P < 0.05) in the milk produced by the cows. There were 29 microbial phyla found in the rumen. The flora of Tenericutes significantly decreased (P < 0.05), Actinobacteria and Planctomycetes significantly increased (P < 0.01), and Spirochaetae significantly increased (P < 0.05) over control. Among the 389 genera of microbes in the rumen, 110 were significantly different (P < 0.05). Comparing to control, Lactobacillus increased significantly (P < 0.01), Enterococcus decreased significantly (P < 0.01), Christensenellaceae R-7-group decreased significantly (P < 0.05), Prevotellaceae-UCG-001 increased significantly (P < 0.05), Lachnospiraceae-UCG-006 decreased significantly (P < 0.01), Lachnospiraceae-NA increased significantly, Butyrivibrio-2 decreased significantly (P < 0.05), and Ruminococcus-1 increased significantly. Conclusion Under the experimental conditions, the dietary supplementation of corn meal and flaxseed oil significantly reduced the fat content in milk of the dairy cows. It did not significantly alter the diversity but significantly changed the structure and abundance of the microbial flora in the cow rumen. The acidogenic as well as starch-utilizing bacteria significantly increased. -
Key words:
- dairy cow /
- milk fat reduction /
- 16S rDNA /
- high-throughput sequencing /
- rumen microbes
-
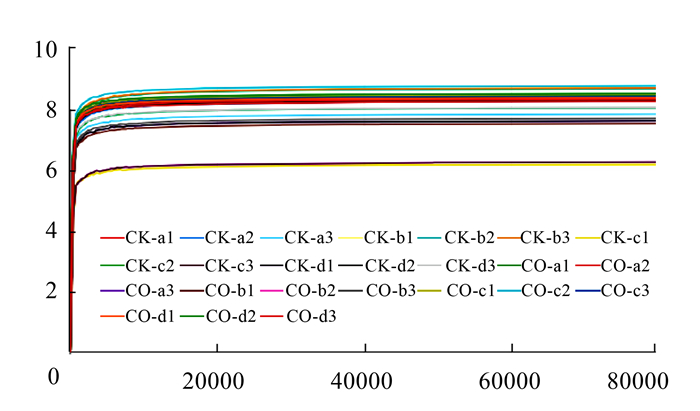
图 2 添加玉米粉和油脂对瘤胃细菌菌群Shannon指数的影响
注:a、b、c、d代表 4头不同的奶牛,每头奶牛瘤胃液样本取3次重复。横坐标表示抽取的tags数量;纵坐标表示抽取一定数量tags时所计算得到的shannon的期望值。
Figure 2. Effect of added corn meal and flaxseed oil in forage on Shannon index of rumen microbial flora
Note: a, b, c, and d represent 4 different cows. Three replicates of rumen secretion sample per cow were applied.The abscissa represents the number of extracted tags; the ordinate represents the expected value of shannon calculated when extracting a certain number of tags.
表 1 奶牛干物质基础日粮组成及营养成分
Table 1. Composition and nutrients of diet for dairy cows on dry matter base
(单位/%) 原料
Ingredient含量
Content日粮营养水平
Dietary nutrition level含量
Content豆粕 Soybean meal 11.30 粗蛋白 CP 17.14 菜籽粕 Rapeseed meal 3.20 钙 Ca 0.76 全棉籽 Whole cottonseed 3.50 磷 P 0.46 麸皮 Wheat bran 3.18 中性洗涤纤维 NDF 35.78 压片玉米 Tablet corn 11.06 淀粉 Corn 24.25 甜菜颗粒 Beet granule 2.49 产奶净能 NEL/(MJ·kg-1) 6.00 啤酒糟 Brewer's grains 3.16 苜蓿青贮 Alfalfa silage 4.12 苜蓿 Alfalfa 10.32 玉米青贮 Corn silage 45.06 碳酸氢钙 Dicalcium phosphate 0.62 石粉 Limestone 0.39 小苏打 Baking soda 0.30 氧化镁 Magnesium oxide 0.50 食盐 Salt 0.30 脱霉素 Demycin 0.10 预混料 Premix 0.40 合计 Total 100.00 注:营养水平中产奶净能为计算值,其他为实测值。
Note: NEL is calculated value; others, measured.表 2 添加玉米粉和油脂粮对奶牛乳成分的影响
Table 2. Effect of added corn meal and flaxseed oil in forage on chemical composition of cow milk
(单位/%) 项目
Item对照组
CK试验组
CO乳脂率 Milk fat 4.05±0.16A 2.10±0.06B 乳蛋白 Milk protein 3.25±0.10a 3.45±0.11a 乳糖 Lactose 4.95±0.21b 5.27±0.08a 注:同行数据肩标不同小写字母表示差异显著(P<0.05),不同大写字母表示差异极显著(P<0.01),表 4~5同。
Note: Different lowercase letters of the peer data shoulders indicate significant difference (P<0.05), and different uppercase letters indicate that the difference is extremely significant (P<0.01).The same as Table 4-5.表 3 样品在0.03距离下的Alpha丰富程度
Table 3. Alpha richness of specimens at distance 0.03
项目
ItemChao1指数
Chao1 indexAce指数
Ace indexShannon指数
Shannon indexSimpson指数
Simpson index覆盖率
Coverage/%对照组 CK 3866.47 3780.21 7.96 0.98 99.29 试验组 CO 3713.57 3642.19 8.35 0.99 99.29 P-value 0.22 0.26 0.16 0.10 - 表 4 添加玉米粉与油脂对瘤胃细菌菌群在门水平上结构的影响
Table 4. Effect of added corn meal and flaxseed oil in forage on makeup of microbial phyla in rumen
(单位/%) 门
Phylum对照组
Mean(CK)试验组
Mean(CO)拟杆菌门 Bacteroidetes 51.91±5.56 54.90±2.18 厚壁菌门 Firmicutes 35.52±2.92 37.85±1.91 变形菌门 Proteobacteria 7.58±4.04 1.34±0.07 Saccharibacteria 0.81±0.15 0.48±0.10 螺旋菌门 Spirochaetae 0.81±0.12b 1.08±0.03a 浮霉菌门 Planctomycetes 0.66±0.10B 1.23±0.18A 软壁菌门 Tenericutes 0.60±0.10a 0.34±0.06b 放线菌门 Actinobacteria 0.44±0.08B 0.99±0.17A 广古菌门 Euryarchaeota 0.18±0.04 0.09±0.03 表 5 添加玉米粉与油脂对瘤胃在属水平上菌群结构的影响
Table 5. Effect of added corn meal and flaxseed oil in forage on makeup of microbial genera in rumen
(单位/%) 属
Genus对照组
Mean(CK)试验组
Mean(CO)肠球菌属 Enterococcus 4.88±1.41A 0.24±0.08B 乳酸杆菌属 Lactobacillus 0.38±0.09B 4.56±0.58A 韦荣球菌属 Veillonellaceae-UCG-001 0.11±0.02A 0.04±0.01B 普雷沃氏菌属 Prevotellaceae-UCG-001 0.70±0.08B 1.21±0.12A 毛螺旋菌属 Lachnospiraceae-UCG-006 0.10±0.01A 0.05±0.01B 瘤胃球菌属-1 Ruminococcus-1 0.12±0.01b 0.26±0.05a 丁酸弧菌属-2 Butyrivibrio-2 0.71±0.09a 0.45±0.07b 克里斯滕森菌属 Christensenellaceae-R-7-group 4.35±0.60a 3.01±0.23b 未注释毛螺旋菌属 Lachnospiraceae-NA 0.55±0.05b 0.91±0.16a -
[1] 赵勐, 卜登攀, 张养东, 等.奶牛乳脂降低综合征理论及其分子调节机制[J].动物营养学报, 2014, 26(2):287-294. doi: 10.3969/j.issn.1006-267x.2014.02.001ZHAO M, BU D P, ZHANG Y D, et al.Milk fat depression in dairy cows:Theories and molecular regulation mechanism[J].Chinese Journal of Animal Nutrition, 2014, 26(2):287-294.(in Chinese) doi: 10.3969/j.issn.1006-267x.2014.02.001 [2] 边四辈.奶牛低乳脂率的原因及解决方法探讨[J].中国奶牛, 2018(6):63-67. http://d.old.wanfangdata.com.cn/Periodical/zgnn201806018BIAN S B. The reasons and solutions of Low-Fat-Concentration milk[J].China Dairy Cattle, 2018(6):63-67.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zgnn201806018 [3] 王建平, 王加启, 卜登攀.精料和饱和脂肪酸对奶牛生产性能和乳中脂肪酸组成的影响[J].中国粮油学报, 2015(1):92-96. http://d.old.wanfangdata.com.cn/Periodical/zglyxb201501017WANG J P, WANG J Q, BU D P.Effects of concentrate and supplemental saturated fatty acid on milk production and milk fatty acid profile of dairy cow[J].Journal of the Chinese Cereals and Oils Association, 2015(1):92-96.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zglyxb201501017 [4] MA L, COOK K L, BAUMAN D E, et al. Short communication:Milk fat depression induced by conjugated linoleic acid and a high-oil and low-fiber diet occurs equally across the day in Holstein cows[J]. Journal of Dairy Science, 2015, 98(3):1851-1855. http://cn.bing.com/academic/profile?id=f855bf2f0098ba96d148cfa0a3e77db8&encoded=0&v=paper_preview&mkt=zh-cn [5] FRUTOS P, TORAL P G, HERVÁS, G. Individual variation of the extent of milk fat depression in dairy ewes fed fish oil:Milk fatty acid profile and mRNA abundance of candidate genes involved in mammary lipogenesis[J]. Journal of Dairy Science, 2017, 100(12):1-12. http://cn.bing.com/academic/profile?id=df384e1da5556eda6af6bea8ed15bd37&encoded=0&v=paper_preview&mkt=zh-cn [6] RAMIREZ RAMIREZ H A, CASTILLO LOPEZ E, HARVATINE K J, et al. Fat and starch as additive risk factors for milk fat depression in dairy diets containing corn dried distillers grains with soluble[J]. Journal of Dairy Science, 2015, 98(3):1903-1914. http://cn.bing.com/academic/profile?id=d33fedf82b68d4c0a4a1edfeb708ca11&encoded=0&v=paper_preview&mkt=zh-cn [7] BELANCHE A, FUENTE G D L, PINLOCHE E, et al. Effect of diet and absence of protozoa on the rumen microbial community and on the representativeness of bacterial fractions used in the determination of microbial protein synthesis[J]. Journal of Animal Science, 2012, 90(11):3924-3936. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=77a74ff75c2409676af5d82cd3de003d [8] GRUBB J A. Effects of an abrupt change in ration from all roughage to high concentrate upon rumen microbial numbers in sheep[J]. Appl Microbiol, 1975, 30(3):404-412. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=PubMed000002140323 [9] HUWS S A, LEE M R F, MUETZEL S M, et al. Forage type and fish oil cause shifts in rumen bacterial diversity[J]. Fems Microbiology Ecology, 2010, 73(2):396-407. http://cn.bing.com/academic/profile?id=e0d82488b4dc87557b92c8e08055deb0&encoded=0&v=paper_preview&mkt=zh-cn [10] NETO A J, MESSANA J D, GRANJA-SALCEDO Y T, et al. Effect of starch level in supplement with or without oil source on diet and apparent digestibility, rumen fermentation and microbial population of Nellore steers grazing tropical grass[J]. Livestock Science, 2017, 202:171-179. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=1f217966deca0edd7fc0f81bfa0a5ea2 [11] WANAPAT M, MAPATO C, PILAJUN R, et al. Effects of vegetable oil supplementation on feed intake, rumen fermentation, growth performance, and carcass characteristic of growing swamp buffaloes[J]. Livestock Science, 2011, 135(1):32-37. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=8fe61274e22b693681092aef091e29f2 [12] WEIMER P J, STEVENSON D M, MERTENS D R. Shifts in bacterial community composition in the rumen of lactating dairy cows under milk fat-depressing conditions[J]. Journal of Dairy Science, 2010, 93(1):265-278. doi: 10.3168/jds.2009-2206 [13] RICO D E, PRESTON S H, RISSER J M, et al. Rapid changes in key ruminal microbial populations during the induction of and recovery from diet-induced milk fat depression in dairy cows[J]. British Journal of Nutrition, 2015, 114(3):358-367. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=BJN114_03\BJN\BJN114_03\S0007114515001865h.xml [14] 朱河水, 王艳玲, 杨国宇, 等.大豆黄酮对奶牛相关产奶性能的影响[J].华北农学报, 2006, 21(6):127-129. doi: 10.3321/j.issn:1000-7091.2006.06.031ZHU H S, WANG Y L, YANG G Y, et al.Effect of daidzein on related lactational performance of dairy cows[J]. Acta Agriculturae Boreali-Sinica, 2006, 21(6):127-129.(in Chinese) doi: 10.3321/j.issn:1000-7091.2006.06.031 [15] SINGH K M, JISHA T K, REDDY B, et al. Microbial profiles of liquid and solid fraction associated biomaterial in buffalo rumen fed green and dry roughage diets by tagged 16S rRNA gene pyrosequencing[J]. Molecular Biology Reports, 2015, 42(1):95-103. doi: 10.1007/s11033-014-3746-9 [16] 刘荣昌, 李英, 孙凤莉, 等.生鲜乳乳糖含量偏高问题的分析与启示[J].中国奶牛, 2014(Z1):42-44. http://d.old.wanfangdata.com.cn/Periodical/zgnn201403010LIU R C, LI Y, SUN F L, et al.Analysis and enlightenment of the problem of high lactose content in raw milk[J]. China Dairy Cattle, , 2014(Z1):42-44.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zgnn201403010 [17] 刘峰, 杜瑞平, 高民.不同粗饲料品质(GI)与不同精料给量水平对奶牛生产性能影响的研究[J].畜牧与饲料科学, 2012, 33(5-6):13-16. http://d.old.wanfangdata.com.cn/Periodical/nmgxmkx201205006LIU F, DU R P, GAO M.Effects of different quality of roughage(GI) and different concentrate supply level on the production performance of dairy cows[J].Animal Husbandry and Feed Science, 2012, 33(5-6):13-16.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/nmgxmkx201205006 [18] RICO D E, HARVATINE K J. Induction of and recovery from milk fat depression occurs progressively in dairy cows switched between diets that differ in fiber and oil concentration[J]. Journal of Dairy Science, 2013, 96(10):6621-6630. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=3d232050ba569b97639b524d7594e879 [19] THANH L P, SUKSOMBAT W. Milk Yield, Composition, and Fatty Acid Profile in Dairy Cows Fed a High-concentrate Diet Blended with Oil Mixtures Rich in Polyunsaturated Fatty Acids[J].Asian-Australasian Journal of Animal Sciences, 2015, 28(6):796-806. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=86e877b0cd11c50b39d418d4ac934ac5 [20] STERK A, JOHANSSON B E O, TAWEEL H Z H, et al. Effects of forage type, forage to concentrate ratio, and crushed linseed supplementation on milk fatty acid profile in lactating dairy cows[J]. Journal of Dairy Science, 2011, 94(12):6078-6091. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=516f155cd6594d84a08314dbae2380c6 [21] GAYNOR P J, WALDO D R, CAPUCO A V, et al. Milk fat depression, the glucogenic theory, and trans-C18:1 fatty acids[J]. Journal of Dairy Science, 1995, 78(9):2008-2015. http://cn.bing.com/academic/profile?id=0d6c904358f0f32363373e356d81ddfe&encoded=0&v=paper_preview&mkt=zh-cn [22] DHIMAN T R, NAM S H, URE A L. Factors Affecting Conjugated Linoleic Acid Content in Milk and Meat[J]. Critical Reviews in Food Science and Nutrition, 2005, 45(6):463-482. doi: 10.1080-10408390591034463/ [23] MAIA M R G, CHAUDHARY L C, FIGUERES L, et al. Metabolism of polyunsaturated fatty acids and their toxicity to the microflora of the rumen[J]. Antonie van Leeuwenhoek, 2007, 91(4):303-314. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=235068efff326d8ed121faccd38f7e67 [24] DEVENDRA C, LEWIS D. The interaction between dietary lipids and fibre in the sheep 2. Digestibility studies[J]. Animal Production, 1974, 19(1):67-76. http://cn.bing.com/academic/profile?id=ea7f621230b06c92aad8cc259cca05f4&encoded=0&v=paper_preview&mkt=zh-cn [25] HENDERSON C. The effects of fatty acids on pure cultures of rumen bacteria[J]. The Journal of Agricultural Science, 1973, 81(1):107-112. doi: 10.1017/S0021859600058378 [26] 李旦.肉牛瘤胃纤维分解菌Real Time PCR定量方法的建立与应用[D].乌鲁木齐: 新疆农业大学, 2007.LI D. Development of application of a Real Time PCR approach for quantification of rumen cellulytic bacateria of cattle[D].Urumchi: Xinjiang Agricultural University, 2007.(in Chinese) [27] HENDERSON C. A Study of the Lipase Produced by Anaerovibrio lipolytica, a Rumen Bacterium[J]. Journal of General Microbiology, 1971, 65(1):81-89. http://cn.bing.com/academic/profile?id=e6a1a2a4e2e3a43cb89b492461e78e20&encoded=0&v=paper_preview&mkt=zh-cn [28] 李旦, 王加启, 卜登攀, 等.运用Real-time PCR方法研究日粮添加豆油与胡麻油对肉牛瘤胃纤维分解菌数量的影响[J].动物营养学报, 2008(3):256-260. doi: 10.3969/j.issn.1006-267X.2008.03.003LI D, WANG J Q, BU D P, et al.Determination of the effects of soybean oil and linseed oil in diets on the quantities of rumen cellulytic bacteria in beef cattle by Real-time PCR[J]. Chinese Journal of Animal Nutrition, 2008(3):256-260.(in Chinese) doi: 10.3969/j.issn.1006-267X.2008.03.003 [29] 张迪.慢性瘤胃酸中毒对瘤胃发酵功能及乳酸代谢菌的影响[D].呼和浩特: 内蒙古农业大学, 2008. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1307648ZHANG D. Effect of subacute rumen acidosis on rumen fermentation and populations of lactate metabolism bacteria[D].Hohhot: Inner Mongolia Agricultural University, 2008.(in Chinese) http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1307648 [30] KREHBIEL C R, STOCK R A, HEROLD D W, et al. Feeding wet corn gluten feed to reduce subacute acidosis in cattle[J]. Journal of Animal Science, 1995, 73(10):2931. doi: 10.2527/1995.73102931x [31] LETTAT A, NOZIōRE, P, SILBERBERG M, et al. Experimental feed induction of ruminal lactic, propionic, or butyric acidosis in sheep1[J]. Journal of Animal Science, 2010, 88(9):3041-3046. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=ab55c2cc7e7fb85e3cff3d62e3f7d543 [32] GRIINARI J M, CORL B A, LACY S H. Conjugated linoleic acid is synthesized endogenously in lactating dairy cows by delta(9)-desaturase[J]. Journal of Nutrition, 2000, 130(9):2285. http://med.wanfangdata.com.cn/Paper/Detail/PeriodicalPaper_PM10958825 [33] 马涛, 刁其玉.瘤胃微生物与饲粮脂肪酸间的相互作用[J].动物营养学报, 2018, 30(5):1611-1618. doi: 10.3969/j.issn.1006-267x.2018.05.001MA T, DIAO Q Y.Interaction between ruminal microbes and dietary fatty acids[J]. Chinese Journal of Animal Nutrition, 2018, 30(5):1611-1618.(in Chinese) doi: 10.3969/j.issn.1006-267x.2018.05.001 [34] HENDERSON G, COX F, GANESH S, et al. Rumen microbial community composition varies with diet and host, but a core microbiome is found across a wide geographical range[J]. Scientific Reports, 2015, 5(1):14567. http://cn.bing.com/academic/profile?id=a383a82abb2cd55c255684cd4f9fff6e&encoded=0&v=paper_preview&mkt=zh-cn [35] TORAL P G, BELENGUER A, SHINGFIELD K J, et al. Fatty acid composition and bacterial community changes in the rumen fluid of lactating sheep fed sunflower oil plus incremental levels of marine algae[J]. Journal of Dairy Science, 2012, 95(2):794-806. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=812debad93df55cf7c8c0f1b8b6301e6 [36] 杨舒黎.日粮添加豆油和胡麻油对奶牛瘤胃细菌及发酵参数的影响[D].北京: 中国农业科学院, 2007. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1057276YANG S L. Effect of soybean oil and linseed oil supplementation on population of ruminal bacteria and fermentation parameters in dairy cows[D].Beijing: Chinese Academy of Agricultural Sciences, 2007.(in Chinese) http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1057276 [37] 姜雅慧, 卜登攀, 杨红建, 等.不饱和脂肪酸在瘤胃氢化的微生物学机制研究进展[J].华北农学报, 2015, 30(S1):376-382. doi: 10.7668/hbnxb.2015.S1.068JIANG Y H, BU D P, YANG H J, et al.The advance research of the microbial biohydrogenation mechanism of unsaturated fatty acid in rumen[J]. Acta Agriculturae Boreali-Sinica, 2015, 30(S1):376-382.(in Chinese) doi: 10.7668/hbnxb.2015.S1.068 [38] 周敏, 叶子弘, 蒋林树.瘤胃氢化多不饱和脂肪酸的影响因素[J].中国农学通报, 2010, 26(8):38-44. http://d.old.wanfangdata.com.cn/Periodical/zgnxtb201008009ZHOU M, YE Z H, JIANG L S.Study of the influencing factor of PUFA living things hydrogenation in rumen[J].Chinese Agricultural Science Bulletin, 2010, 26(8):38-44.(in Chinese) http://d.old.wanfangdata.com.cn/Periodical/zgnxtb201008009 -







 下载:
下载: